Moderna anuncia los primeros participantes que recibieron dosis en la tercera fase del ensayo clínico
Moderna anuncia los primeros participantes que recibieron dosis en la tercera fase del ensayo clínico para su vacuna contra la influenza estacional (mRNA-1010)
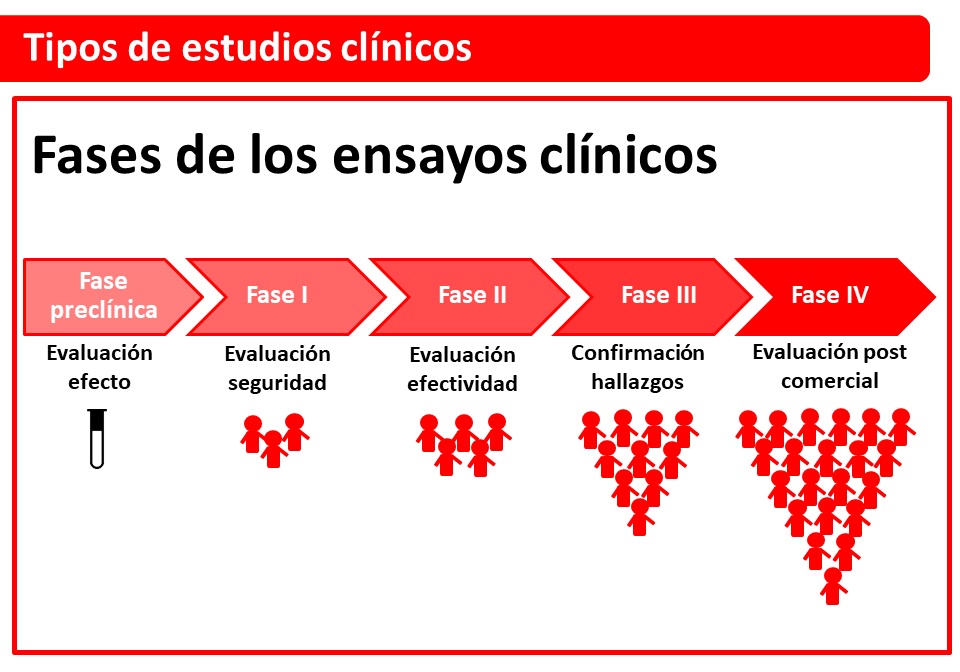
mRNA-1010 es el primer candidato a vacuna contra la influenza estacional de Moderna que ingresa a un ensayo de Fase 3.
· mRNA-1010 es una de varias vacunas candidatas contra la influenza que se están desarrollando en la cartera respiratoria de Moderna.
· Moderna ahora tiene cuatro programas en estudios de fase 3: refuerzo COVID bivalente conteniendo Ómicron, influenza, RSV, CMV.
REPÚBLICA DOMINICANA, 7 de junio, 2022 / Moderna, Inc. (NASDAQ:MRNA), una compañía de biotecnología pionera en terapias y vacunas de ARN mensajero (ARNm), anunció hoy que los primeros participantes de un estudio de fase 3 de la vacuna candidata contra la influenza estacional de la compañía (mRNA-1010) recibieron sus dosis. Se espera que el ensayo inscriba a aproximadamente 6000 adultos en los países del hemisferio sur.
«Nos complace comenzar este estudio de Fase 3 de nuestra vacuna candidata contra la influenza estacional, mRNA-1010, nuestra cuarta vacuna candidata de ARNm para comenzar un estudio fundamental de Fase 3. mRNA-1010 es la primera de varias vacunas candidatas contra la influenza que estamos desarrollando con el objetivo de mejorar iterativamente las vacunas tradicionales mediante la inducción de respuestas inmunitarias amplias y sólidas. Creemos que nuestra plataforma de ARNm, con la flexibilidad y la velocidad de nuestro proceso de fabricación, está bien posicionada para abordar la importante necesidad insatisfecha en la gripe estacional», dijo Stephan Bancel, director ejecutivo de Moderna.
Según Bancel, las vacunas contra la influenza son un pilar clave en la estrategia de vacunas respiratorias, que incluye el desarrollo de candidatos combinados dirigidos a múltiples virus en una sola vacuna, incluida la influenza con SARS-CoV-2 y el virus respiratorio sincitial. Con el inicio de la dosificación para su programa mRNA-1010, Moderna ahora tiene cuatro programas en estudios de Fase 3 de etapa tardía, incluido su refuerzo SARS-CoV-2, RSV, gripe estacional y vacunas contra la CMV. A partir de otoño del 2022, la plataforma de la fase 3 de la compañía podría dar lugar a tres lanzamientos respiratorios comerciales en los próximos dos o tres años.
Este estudio aleatorizado y ciego al observador de fase 3 está diseñado para evaluar la seguridad y la no inferioridad inmunológica de mRNA-1010 frente a una vacuna contra la influenza estacional autorizada en adultos de 18 años o más. Los participantes serán asignados al azar en una proporción de 1:1 para recibir una dosis única de mRNA-1010 o una dosis única de una vacuna contra la influenza estacional autorizada como comparación.
Acerca de mRNA-1010 e Influenza Estacional
mRNA-1010 es una vacuna candidata que codifica las glicoproteínas de hemaglutinina (HA) de las cuatro cepas de influenza recomendadas por la Organización Mundial de la Salud (OMS) para la prevención de la influenza, incluida la influenza A/H1N1, A/H3N2 y los linajes de influenza B/Yamagata- y B/Victoria-. La HA es una de las principales glicoproteínas de superficie de la influenza, que se considera un blanco importante para generar una amplia protección contra la influenza, y es el objetivo principal de las vacunas contra la influenza actualmente disponibles. Moderna se está preparando de manera proactiva para un estudio de eficacia confirmatorio para mRNA-1010 tan pronto como a la temporada de influenza del hemisferio norte 2022/2023, de ser necesario.
Las epidemias de influenza (influenza A e influenza B) ocurren estacionalmente y varían en severidad cada año, causando enfermedades respiratorias y suponiendo una carga considerable para los sistemas de atención médica. La influenza provoca anualmente de 3 a 5 millones de casos graves de influenza, y de 290 000 a 650 000 muertes respiratorias relacionadas con la influenza en todo el mundo, a pesar de la actual disponibilidad de vacunas contra la influenza. A pesar de que tanto la influenza A como la B causan epidemias estacionales, son los virus de la influenza A los que provocan >95% de las hospitalizaciones relacionadas con la influenza en adultos.
Programa de vacunación respiratoria de Moderna
Moderna está avanzando en una cartera de candidatos respiratorios, incluidos cinco candidatos a vacunas de ARNm contra la influenza. Además de mRNA-1010, Moderna está desarrollando vacunas candidatas contra la influenza que incluyen antígenos HA adicionales para una cobertura más amplia de las cepas de influenza A circulantes (mRNA-1011 y mRNA-1012) y vacunas candidatas que incorporan antígenos HA y neuraminidasa (NA) para apuntar a múltiples proteínas involucradas en el ciclo de vida del virus de la influenza, para reducir el potencial de escape antigénico viral (mRNA-1020 y mRNA-1030).
Moderna también está desarrollando dos vacunas candidatas combinadas, incluida una vacuna candidata contra la influenza y el SARS-CoV-2 (mRNA-1073), y otra candidata contra la influenza, el SARS-CoV-2 y el RSV (mRNA-1230). El objetivo de las vacunas candidatas combinadas de Moderna es brindar protección contra múltiples patógenos respiratorios en una sola vacuna.
Acerca de Moderna
Durante más de 10 años desde su inicio, Moderna se ha transformado de una empresa de etapa de investigación que promueve programas en el campo del ARN mensajero (ARNm) a una empresa con una diversa cartera clínica de vacunas y terapias en siete modalidades, una amplia cartera de propiedad intelectual en áreas que incluyen ARNm y formulación de nanopartículas de lípidos, y una planta de fabricación integrada que permite una rápida producción clínica y comercial a escala.
Moderna mantiene alianzas con una amplia gama de colaboradores gubernamentales y comerciales nacionales y extranjeros, lo que ha permitido la búsqueda tanto de ciencia innovadora como de un rápido crecimiento en la fabricación. Más recientemente, las capacidades de Moderna se unieron para permitir el uso autorizado y la aprobación de una de las primeras y más efectivas vacunas contra la pandemia de COVID-19.
La plataforma de ARNm de Moderna se basa en los avances continuos de la ciencia básica y aplicada del ARNm y la tecnología de distribución y fabricación. Esto ha permitido el desarrollo de terapias y vacunas para enfermedades infecciosas, inmuno-oncología, enfermedades raras, enfermedades cardiovasculares y enfermedades autoinmunes. Moderna ha sido nombrada uno de los principales empleadores biofarmacéuticos por Science durante los últimos siete años. Para obtener más información, visite www.modernatx.com.
Declaraciones a futuro
Este comunicado de prensa contiene declaraciones a futuro dentro del significado de la Ley de Reforma de Litigios de Valores Privados de 1995 y sus enmiendas, incluida la inscripción prevista en el ensayo de Fase 3 de mRNA-1010; el potencial de las vacunas contra la influenza de Moderna de mejorar las vacunas tradicionales contra la influenza; los planes de Moderna con respecto a un posible estudio de confirmación de eficacia para mRNA-1010; y el potencial para brindar protección contra múltiples patógenos respiratorios en una sola vacuna.
Las declaraciones a futuro en este comunicado de prensa no son promesas ni garantías, y no se debe confiar indebidamente en estas declaraciones a futuro porque involucran riesgos conocidos y desconocidos, incertidumbres y otros factores, muchos de los cuales están fuera del control de Moderna, lo que podría causar que los resultados reales difieran materialmente de los implícitos o expresados en estas declaraciones.
Estos riesgos, incertidumbres y otros factores incluyen aquellos riesgos e incertidumbres descritos bajo el título «Factores de riesgo» en el Informe anual más reciente de Moderna en el Formulario 10-K, presentado ante la Comisión de Bolsa y Valores de EE. UU. (SEC), y en presentaciones posteriores realizadas por Moderna con la SEC, disponibles en el sitio web de la SEC en www.sec.gov. Salvo que lo exija la ley, Moderna renuncia a cualquier intención o responsabilidad de actualizar o revisar las declaraciones a futuro contenidas en este comunicado de prensa en caso de nueva información, desarrollos futuros u otros. Estas declaraciones a futuro se basan en las expectativas actuales de Moderna y se refieren únicamente a la fecha del presente.